Sepsis ist die Summe lebensbedrohlicher Krankheitssymptome und pathophysiologischer Veränderungen, verursacht durch Keime (Bakterien, Viren, Pilze oder Parasiten) und deren Produkte (PAMPs, pathogen-associated microbial patterns), die aus einem Infektionsherd in die Blutbahn eindringen. Der Körper reagiert mit der Bildung endogener Mediatoren (Zytokine), die Entzündungskaskaden aktivieren. Diese führen zu einer nicht mehr kontrolliert ablaufenden systemischen Entzündungsreaktion.
Zellbasiertes Testsystem zum Nachweis pyrogener Rückstände
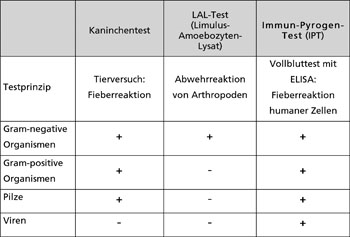
PAMPs, Überreste oder isolierte Strukturen von bakteriellen Erregern wie Zellwandbestandteile von Mikroorganismen, können in der Klinik und an medizintechnischen Produkten auftreten. Medizinische Geräte, die Kontakt zum Blutkreislauf oder zu großflächig verletztem Gewebe haben, müssen auf solch pyrogene Rückstände untersucht werden. Derzeit gibt es drei kommerzielle Methoden für den Nachweis von Pyrogenen (Tabelle 1). Sie sind entweder sehr aufwändig, umstritten oder nur auf bestimmte Pyrogene beschränkt.
Neuer colorimetrischer Assay
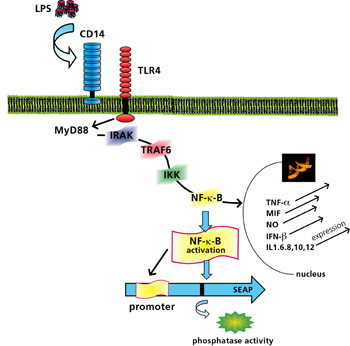
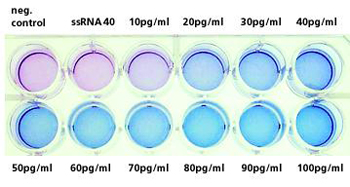
Am Fraunhofer IGB haben wir ein neues zellbasiertes Testsystem entwickelt, das die Identifizierung und Differenzierung von PAMPs über Toll-like Rezeptoren (TLRs) [3, 4] ermöglicht (Patent angemeldet). Es ist als colorimetrischer TLR-induzierter Reportergen-Assay konzipiert (Bild 1), bei dem positive Proben anhand einer Farbreaktion leicht erkennbar sind (Bild 2).
Für den Assay wurde der Rezeptorkomplex Toll-like-Rezeptor 4 mit Corezeptor CD14 (MD2) über Plasmide in NIH-3T3-Fibroblasten, die das Reportergen enthalten, transfiziert und exprimiert. Die Induktion der TLRs durch ein Endotoxin (Referenzsubstanz Lipopolysaccharid, LPS) führt nach einer Signalkaskade zur Aktivierung des Transkriptionsfaktors NF-kB, welcher die Expression des Reportergens, einer sezernierten alkalischen Phosphatase (SEAP), kontrolliert. Bei positiven Proben entsteht durch Substratzugabe ein tiefblau gefärbter, unlöslicher und mit bloßem Auge leicht erkennbarer Niederschlag.
Vorteile
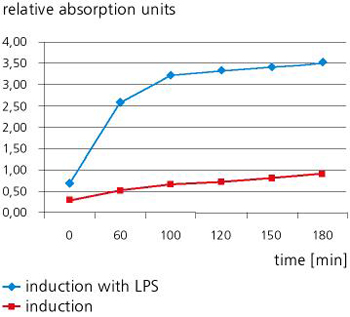
Mit dem in unserem Labor entwickelten Testsystem können Pyrogene schnell, einfach und ohne großen apparativen Aufwand nachgewiesen werden – qualitativ und quantitativ. Da mit dem neuen Testsystem alle relevanten pyrogenen, Sepsis verursachenden Substanzen detektiert und verifiziert werden können, ist es sowohl in der medizinischen Diagnostik als auch in der Medizintechnik optimal einsetzbar.
Anwendungen und Ausblick
Das neue Testsystem kann bisherige Tests wie LAL und IPT ergänzen oder ersetzen. Pyrogene können an medizinischen Geräten, injizierbaren Arzneimitteln und an Implantaten oder Instrumenten etc. nachgewiesen werden. Weitere Anwendungen sind denkbar in der Lebensmittelindustrie (Pyrogene in Nahrungsmitteln) und der Pharmaindustrie (Pyrogene in Medikamenten). TLR-Antagonisten finden zunehmend Einsatz in der Dermatologie.
Wir wollen das Testverfahren um die TLRs 1-10 erweitern, um damit alle PAMPs selektiv zu erkennen und zu identifizieren.
Literatur
[1] Werner-Felmayer, G., Baier-Bitterlich, G., Fuchs, D., Hausen, A., Murr, C., Reibnegger, G., Werner, E. R., Wachter, H. (1995). Detection of bacterial pyrogens on the basis of their effects on gamma interferon-mediated formation of neopterin or nitrite in cultured monocyte cell lines. Clinical and diagnostic laboratory immunology 2(3); 307-313.
[2] J.Jorgensen, J., Alexander, G. A. (1982). Rapid detection of significant bacteriuria by use of an automated Limulus amoebocyte lysat assay. Journal of clinical Microbiology 16(3); 587-589. [12] Akira,S. (2003). Toll-like receptor signaling. J.Biol.Chem. 278, 38105-38108.
[3] Lakhani SA, Bogue CW. (2003). Toll-like receptor signaling in sepsis. Curr Opin Pediatr. 15(3):278-82.
[4] Undurti N. Das. (2003). Current advances in sepsis and septic shock with particular emphasis on the role of insulin. Med Sci Monit 9(8): Ra181-192.
 Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB
Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB